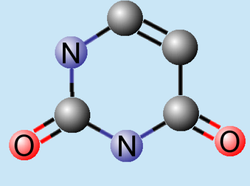
NOMENCLATURA
METODO DE OBTECION
Se describe un procedimiento para la preparaci
on
de 9 - (2 - hidroxietoximetil) guanina (Acyclo-
vir) mediante tratamiento de cloruro de 2 - ben-
zoiloxietoximetilo y N,2 - acetil guanina y elimi-
naci
on posterior de los grupos acetilo y benzoilo
por hidrazinolisis.https://www.google.com/search?q=NOMENCLATURA+DE+GUANINA&client=firefox-b&biw=1366&bih=631&noj=1&source=lnms&tbm=isch&sa=X&ved=0ahUKEwjYm4rv7pzPAhWDVyYKHTBjBIAQ_AUICCgB#imgrc=tFKOeu7X1CIB3M%3Ahttp://www.espatentes.com/pdf/2007988_a6.pdf